Química pura:
Que se encarga del estudio de las substancias orgánicas y las substancias inorgánicas. Se divide en:
- Química orgánica: Estudia la materia viviente.
- Química inorgánica: Estudia la materia sin vida.
- Química analítica: Su finalidad es el estudio de un material o muestra mediante diferentes métodos.
- Físico-química: Estudia los fenómenos comunes a estas 2 ciencias.
- Química preparativa: Preparación y purificación de substancias en el laboratorio para el desarrollo de nuevos productos.
Química aplicada:
Estudia los procedimientos de la química pura para resolver problemas de las distintas áreas. Se divide en:
- Quimiurgia: Estudia la aplicación de la química en la agricultura con vistas a su utilización como materia prima en otras industrias.
- Bioquímica: Estudia los procesos químicos que ocurren en los seres vivos.
- Astroquímica: Estudia la composición sustancial existente en el universo. Es la ciencia que se ocupa de la composición química del Sol y de los planetas, de las estrellas y de la materia difusa interplanetaria o, más en general, interestelar.
- Cristaloquímica: Sobre la relación entre la composición química y las propiedades y formas de cristalización de las sustancias.
- Química Farmacéutica: Estudia la estructura, propiedades y aplicaciones de los medicamentos.
- Química técnica o industrial: Trata de la obtención de sustancias en operaciones generales o unitarias o cada industria en particular.
Química orgánica
La química orgánica o química del carbono es la rama de la química que estudia una clase numerosa de moléculas que contienen carbono formando enlaces covalentes carbono-carbono o carbono-hidrógeno y otros heteroátomos, también conocidos como compuestos orgánicos. Friedrich Wöhler y Archibald Scott Couperson conocidos como los padres de la química orgánica.
Historia
La química orgánica se constituyó como disciplina en los años treinta. El desarrollo de nuevos métodos de análisis de las sustancias de origen animal y vegetal, basados en el empleo de disolventes como el éter o el alcohol, permitió el aislamiento de un gran número de sustancias orgánicas que recibieron el nombre de "principios inmediatos". La aparición de la química orgánica se asocia a menudo al descubrimiento, en 1828, por el químico alemán Friedrich Wöhler, de que la sustancia inorgánica cianato de amonio podía convertirse en urea, una sustancia orgánica que se encuentra en la orina de muchos animales. Antes de este descubrimiento, los químicos creían que para sintetizar sustancias orgánicas, era necesaria la intervención de lo que llamaban ‘lafuerza vital’, es decir, los organismos vivos. El experimento de Wöhler rompió la barrera entre sustancias orgánicas e inorgánicas. Los químicos modernos consideran compuestos orgánicos a aquellos que contienen carbono e hidrógeno, y otros elementos (que pueden ser uno o más), siendo los más comunes: oxígeno, nitrógeno, azufre y los halógenos.
La diferencia entre la química orgánica y la química biológica es que en la química biológica las moléculas de ADN tienen una historia y, por ende, en su estructura nos hablan de su historia, del pasado en el que se han constituido, mientras que una molécula orgánica, creada hoy, es sólo testigo de su presente, sin pasado y sin evolución histórica.1
Cronología
- 1675: Lémerg clasifica los productos químicos naturales, según su origen en minerales, vegetales y animales
- 1784: Antoine Lavoisier demuestra que todos los productos vegetales y animales están formados básicamente porcarbono e hidrógeno y, en menor proporción, nitrógeno, oxígeno y azufre
- 1807: Jöns Jacob Berzelius clasifica los productos químicos en:
- Orgánicos: los que proceden de organismos vivos.
- Inorgánicos: los que proceden de la materia inanimada.
- 1816: Michel Eugène Chevreul prepara distintos jabones a partir de diferentes fuentes de ácidos grasos y diversas bases, produciendo así distintas sales de ácidos grasos (o jabones), que no resultaron ser más que productos orgánicos nuevos derivados de productos naturales (grasas animales y vegetales).
- 1828: Friedrich Wöhler sintetiza a partir de sustancias inorgánicas y con técnicas normales de laboratorio, creó la sustancia Urea, la segunda sustancia orgánica obtenida artificialmente, luego del oxalato de amonio.
Primeros compendios
La tarea de presentar la química orgánica de manera sistemática y global se realizó mediante una publicación surgida en Alemania, fundada por el químico Friedrich Konrad Beilstein (1838-1906). Su Handbuch der organischen Chemie (Manual de la química orgánica) comenzó a publicarse en Hamburgo en 1880 y consistió en dos volúmenes que recogían información de unos quince mil compuestos orgánicos conocidos. Cuando la Deutsche chemische Gesellschaft (Sociedad Alemana de Química) trató de elaborar la cuarta re-edición, en la segunda década del siglo XX, la cifra de compuestos orgánicos se había multiplicado por diez. Treinta y siete volúmenes fueron necesarios para la edición básica, que aparecieron entre 1916 y 1937. Un suplemento de 27 volúmenes se publicó en 1938, recogiendo información aparecida entre 1910 y 1919. En la actualidad, se está editando el Fünftes Ergänzungswerk (quinta serie complementaria), que recoge la documentación publicada entre 1960 y 1979. Para ofrecer con más prontitud sus últimos trabajos, el Beilstein Institut ha creado el servicio Beilstein Online, que funciona desde 1988. Recientemente, se ha comenzado a editar periódicamente un CD-ROM, Beilstein Current Facts in Chemistry, que selecciona la información química procedente de importantes revistas. Actualmente, la citada información está disponible a través de internet.
El alma de la Química orgánica: El Carbono
La gran cantidad de compuestos orgánicos que existen tiene su explicación en las características del átomo de carbono, que tiene cuatro electrones en su capa de valencia: según la regla del octeto necesita ocho para completarla, por lo que forma cuatro enlaces(valencia = 4) con otros átomos. Esta especial configuración electrónica da lugar a una variedad de posibilidades de hibridación orbital del átomo de Carbono (hibridación química).
Véase también: Hibridación (química)
Véase también: Estructura de Lewis
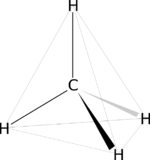
La molécula orgánica más sencilla que existe es el Metano. En esta molécula, el Carbono presenta hibridación sp3, con los átomos de hidrógeno formando un tetraedro.
El carbono forma enlaces covalentes con facilidad para alcanzar una configuración estable, estos enlaces los forma con facilidad con otros carbonos, lo que permite formar frecuentemente cadenas abiertas (lineales o ramificadas) y cerradas (anillos)